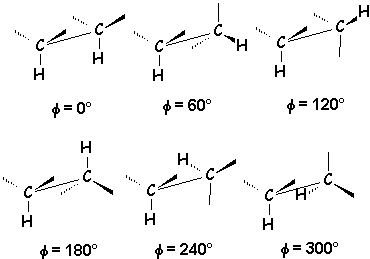
Conformations de l’éthane.
On appelle conformation d'une molécule les différentes structures spatiales qu'elle peut prendre par suite de rotations autour d'une ou plusieurs liaisons simples C-C.
La valeur de l’énergie potentielle de la molécule varie en fonction de l’angle dičdre j entre deux liaisons C ľ H prises comme référence. Elle est de l’ordre de 12 kJ lorsque les atomes sont en vis-ŕ-vis.
 |
La variation de l’énergie potentielle en fonction de j est :

il y a 3 molécules en conformation éclipsée (vis-ŕ-vis). (on a les męmes conformations pour j = 0°, 120°, 240° et j = 60°, 180°, 300°, ces trois derničres étant des conformations décalées)